Un espectro continuo en luz visible
El espectro continuo se atribuye a la agitación térmica de los átomos, que en el cuerpo sólido ocupan posiciones bien determinadas de equilibrio, alrededor de las cuales vibran con mayor energía cuanto mayor es la temperatura del cuerpo. En estos espectros no se observan rayas o zonas oscuras o negras. Se producen cuando la fuente luminosa es un sólido o liquido incandescente.
ESPECTRO DISCONTINUO
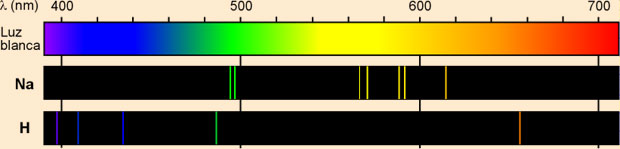
En el siglo XVII, Isaac Newton demostró que la luz blanca visible procedente del sol puede descomponerse en sus diferentes colores mediante un prisma. El espectro que se obtiene es continuo; contiene todas las longitudes de onda desde el rojo al violeta, es decir, entre unos 400 y 700 nm (1 nm -nanómetro- = 10-9 m).
En cambio la luz emitida por un gas incandescente no es blanca sino coloreada y el espectro que se obtiene al hacerla pasar a través de un prisma es bastante diferente. Es un espectro discontinuo que consta de líneas o rayas emitidas a longitudes de onda específicas. Cada elemento (es decir cada tipo de átomos) posee un espectro característico que puede utilizarse para identificarlo. Por ejemplo, en el del sodio, hay dos líneas intensas en la región amarilla a 589 nm y 589,6 nm.
Uno de los espectros atómicos más sencillos, y que más importancia tuvo desde un punto de vista teórico, es el del hidrógeno. Cuando los átomos de gas hidrógeno absorben energía por medio de una descarga de alto voltaje, emiten radiaciones que dan lugar a 5 líneas en la región visible del espectro:
En cambio la luz emitida por un gas incandescente no es blanca sino coloreada y el espectro que se obtiene al hacerla pasar a través de un prisma es bastante diferente. Es un espectro discontinuo que consta de líneas o rayas emitidas a longitudes de onda específicas. Cada elemento (es decir cada tipo de átomos) posee un espectro característico que puede utilizarse para identificarlo. Por ejemplo, en el del sodio, hay dos líneas intensas en la región amarilla a 589 nm y 589,6 nm.
Uno de los espectros atómicos más sencillos, y que más importancia tuvo desde un punto de vista teórico, es el del hidrógeno. Cuando los átomos de gas hidrógeno absorben energía por medio de una descarga de alto voltaje, emiten radiaciones que dan lugar a 5 líneas en la región visible del espectro:
 |
| El modelo atómico de Rutherford no podía explicar estas emisiones discretas de radiación por los átomos. Además presentaba el inconveniente de ser inestable: Según la física clásica una carga en movimiento emite continuamente energía por lo que los electrones radiarían energía continuamente hasta "caer" en el núcleo, con lo que el átomo se destruiría. |


O, no podias escoger una letra menos mareante??
ResponderEliminarme encanto! yo sigo química en el bachillerato y tu información me ayudo muchísimo. Muy fácil de entender (pongas la letra que pongas -.-´)
ResponderEliminarmuy buena información, eso si linda, puedes poner una letra mas legible, eso muchas gracias.
ResponderEliminarla letra que fuente es?
ResponderEliminares buena tu info pero nmms tu letra es otro pedo
ResponderEliminarjaja apenas lo ví
ResponderEliminar